- In:
- Posted By: Capuano Edoardo
- Commenti: 0
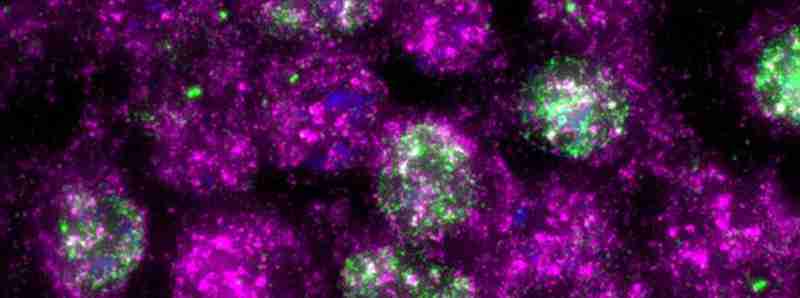
Il danno da radiazioni UV porta a blocchi stradali sui ribosomi, causando la morte precoce delle cellule della pelle
In uno studio recente, i ricercatori della Johns Hopkins Medicine suggeriscono che l’RNA messaggero (mRNA) della cellula – il principale traduttore e regolatore del materiale genetico – insieme a una proteina critica chiamata ZAK, stimolano la risposta iniziale della cellula ai danni delle radiazioni UV e svolgono un ruolo fondamentale se la cellula vive o muore.
Sebbene sia noto da tempo che le radiazioni UV danneggiano il DNA, come pure l'mRNA, e gli ultimi risultati, pubblicati su Cell (1), indicano che gli mRNA agiscono come primi soccorritori dicendo alle cellule come gestire lo stress.
«L’RNA è un canarino nella miniera di carbone. Sta dicendo alla cellula: 'Abbiamo gravi danni qui e dobbiamo fare qualcosa'», afferma la dottoressa Rachel Green, Ph.D. (2), una illustre professoressa di biologia molecolare e genetica di Bloomberg e del Department of Molecular Biology and Genetics presso la Johns Hopkins University School of Medicine. Ella è anche ricercatrice presso l'Howard Hughes Medical Institute (HHMI)
ZAK è un'attrice chiave in un processo che identifica il danno cellulare rilevando le collisioni dei ribosomi, minuscole macchine macromolecolari che aiutano l'RNA a tradurre il linguaggio dei geni nel linguaggio delle proteine. Le collisioni si verificano quando i ribosomi si muovono lungo gli mRNA danneggiati dai raggi UV e, incapaci di decodificare il messaggio danneggiato, fanno sì che i ribosomi bloccati vengano “retroposti” dai ribosomi a monte. Le collisioni ribosomiali attivano ZAK, che innesca un programma di segnalazione cellulare noto come risposta allo stress ribotossico. ZAK poi innesca una cascata di eventi a valle che decidono il destino della cellula.
«Una comprensione più completa di come vengono prese le decisioni sulla vita e sulla morte cellulare quando si incontra la radiazione UV potrebbe aiutare i ricercatori a comprendere le cause alla base del cancro della pelle e di altri tumori», afferma il dottor Niladri Sinha, Ph.D. (3), Jane Coffin Childs Memorial Fund Postdoctoral Fellow presso la Johns Hopkins School of Medicine. «Le aziende sviluppatrici di farmaci mirati per i ribosomi potrebbero anche scoprire che ZAK fungerebbe da motore della morte cellulare in tutti i tipi di cancro», dice.
«I risultati indicano che ZAK rileva l'entità del danno cellulare e risponde a seconda della quantità di radiazioni UV che la cellula riceve, offrendo una comprensione della morte cellulare causata dai raggi UV e identificando nuovi modi per mantenere sotto controllo l'attività di ZAK», afferma Green.
«Ci sono modi graduali in cui ZAK risponde», afferma.
«La ricerca mostra anche molto chiaramente che, ad esempio, il destino di una cellula della pelle subito dopo la radiazione UV è determinato principalmente dall'entità della collisione dei ribosomi e dalla segnalazione ZAK», afferma la professoressa Green.
«In questo regime, il danno al DNA e il percorso di risposta al danno al DNA ben caratterizzato, inclusa la proteina chiave p53, non determinano in modo significativo le decisioni sul destino cellulare. La riparazione del danno al DNA è fondamentale e avviene in un sottoinsieme di cellule che copiano il loro materiale genetico, ma questi percorsi non sono i principali “decisori” del destino cellulare», spiega la professoressa Green.
Rachel Green ha co-guidato la ricerca con il dottor Sergi Regot, Ph.D. (4), professore associato di biologia molecolare e genetica presso la Johns Hopkins University School of Medicine, e il dottor Alban Ordureau, Ph.D., (5) assistente membro del Programma di biologia cellulare al Memorial Sloan Kettering Institute del Kettering Cancer Center e professore assistente alla Weill Cornell.
Per condurre la loro ricerca, gli scienziati hanno esposto modelli cellulari umani a una lampada UV che imitava la radiazione solare. Utilizzando la proteomica per comprendere la segnalazione cellulare in un approccio guidato dal professor Ordureau, hanno valutato il ruolo di ZAK e fatto previsioni su come le cellule avrebbero risposto a diversi livelli di stress. Da lì, gli esperimenti di imaging di cellule vive condotti da Regot, oltre alla biochimica interna dei ribosomi – il cavallo di battaglia del laboratorio di Green – hanno contribuito a caratterizzare il modo in cui la morte cellulare viene regolata come conseguenza della radiazione UV mediata da ZAK.
«In futuro, i ricercatori intendono studiare tipi di cellule con diversi regimi di sintesi proteica, compresi quelli del melanoma e di altri tumori. I ricercatori sospettano che le cellule in rapida crescita si affideranno alla regolazione mediata da ZAK più di altre», conclude la dottoressa Green.
Il finanziamento per questa ricerca è stato fornito dall'Howard Hughes Medical Institute, dal National Institutes of Health (NIH 1R35GM133499), da una borsa di studio per la carriera della National Science Foundation, dal Jane Coffin Childs Memorial Fund for Medical Research Fellowship e dal National Institute of General Medical Sciences, i fondi per l'avvio dello Sloan Kettering Institute, il Pew Charitable Trusts, una sovvenzione di sostegno al Memorial Sloan Kettering Cancer Center e il Programma di ricerca scientifica di base della National Research Foundation of Korea; Ministero della Pubblica Istruzione.Altri scienziati che hanno contribuito a questo studio sono Connor McKenney, Zhong Y. Yeow e Jeffrey J. Li della Johns Hopkins; Ki Hong Nam dello Sloan Kettering Institute del Memorial Sloan Kettering Cancer Center; e Tomer M. Yaron-Barir, Jared L. Johnson, Emily M. Huntsman e Lewis C. Cantley di Weill Cornell Medicine.
Green è membro del comitato consultivo scientifico di Alltrna, Inizial Therapeutics e Arrakis Pharmaceuticals, è consulente per Vertex Pharmaceuticals, Bristol-Myers Squibb (Celgene), Monta Rosa Therapeutics e Flagship Pioneering e ha fatto parte del comitato consultivo scientifico di Moderna. Green, Regot, Sinha e McKenney hanno depositato un brevetto relativo al lavoro descritto in questa ricerca.
Riferimenti:
(1) The ribotoxic stress response drives UV-mediated cell death
(2) Rachel Green
(3) Niladri Sinha
(4) Sergi Regot
(5) Alban Ordureau
Descrizione foto: Il danno da radiazioni UV può costringere una cellula danneggiata a decidere tra la sopravvivenza e il suicidio cellulare. Una nuova ricerca del laboratorio di Rachel Green mostra che il DNA non è l'unico fattore scatenante. Immediatamente dopo l'esposizione ai raggi UV, i ribosomi attivano un diffuso percorso di vita o di morte (rosa), che è più pervasivo della risposta avviata dal DNA (verde). - Credit: Zhong Yeow e Niladri Sinha.
Autore traduzione riassuntiva e adattamento linguistico: Edoardo Capuano / Articolo originale: UV Radiation Damage Leads to Ribosome Roadblocks, Causing Early Skin Cell Death
