- In:
- Posted By: Capuano Edoardo
- Commenti: 0
Scoperta la causa per cui alcune parti del cervello sono particolarmente vulnerabili ai danni neurologici causati dall'Alzheimer
La perdita di memoria è spesso il primo segno della malattia di Alzheimer, seguita da confusione e difficoltà di pensiero. Questi sintomi riflettono il modello tipico di peggioramento del danno ai tessuti cerebrali. I gruppi tossici di proteine si concentrano prima nei lobi temporali del cervello - l'area della memoria - prima di diffondersi in parti del cervello importanti per il pensiero e la pianificazione.
Uno studio condotto da ricercatori della Washington University School of Medicine di Saint Louis fornisce indizi sul motivo per cui alcune parti del cervello sono particolarmente vulnerabili ai danni dell'Alzheimer. Si riduce al gene APOE (apolipoproteina E), il più grande fattore di rischio genetico per la malattia di Alzheimer. Le parti del cervello in cui l'APOE è più attivo sono le aree che subiscono il maggior danno, hanno scoperto.
I risultati, pubblicati su Science Translational Medicine (1), aiutano a spiegare perché i sintomi dell'Alzheimer a volte variano e sottolineano un aspetto poco studiato dell'Alzheimer che suggerisce che meccanismi biologici ancora da scoprire potrebbero svolgere un ruolo importante nella malattia.
Il dottor Brian A. Gordon, PhD, (2) autore senior e assistente professore di radiologia presso il Mallinckrodt Institute of Radiology della School of Medicine (3), spiega: «Ci sono alcune forme rare e atipiche di Alzheimer in cui le persone sviluppano prima problemi di linguaggio o di vista piuttosto che problemi di memoria. Quando esamini i loro cervelli, vedi danni al linguaggio o alle aree visive, e non tanto alle aree della memoria. Le persone con Alzheimer atipico sono spesso escluse dagli studi di ricerca perché è più facile studiare un gruppo in cui tutti hanno lo stesso insieme di sintomi. Ma questa eterogeneità ci dice che ci sono cose che ancora non capiamo su come e perché l'Alzheimer si sviluppa in quel modo. C'è una ragione per cui alcune aree cerebrali vengono danneggiate e altre no, e non conosciamo ancora quella ragione. Ogni mistero che scopriamo con questa malattia ci avvicina a ciò di cui abbiamo bisogno per affrontarla».
La malattia di Alzheimer inizia con una proteina del cervello nota come amiloide-beta. La proteina inizia a formarsi in placche in un arco di tempo di circa due decenni o anche prima che le persone mostrino i primi segni di problemi neurologici. Dopo anni di accumulo di amiloide, iniziano a formarsi grovigli di tau, un'altra proteina del cervello. Subito dopo, i tessuti nelle aree colpite iniziano ad appassire e morire, e inizia il declino cognitivo.
Per capire perché il danno cerebrale dell'Alzheimer si verifica e dove si verifica, Gordon e colleghi - tra cui il primo autore Aylin Dincer, un tecnico del laboratorio di Gordon - hanno studiato 350 persone che si sono offerte come volontarie per studi sulla memoria e sull'invecchiamento attraverso la malattia di Alzheimer, con l'assistenza di Charles F. e Joanne Knight della School of Medicine. I partecipanti sono stati sottoposti a scansioni cerebrali in modo che i ricercatori potessero misurare la quantità e la posizione delle placche amiloidi e dei grovigli di tau e i volumi di varie aree cerebrali.
I ricercatori hanno confrontato i pattern dei gruppi proteici e del danno tissutale nei volontari con i pattern di espressione genica dell'APOE e di altri geni associati al morbo di Alzheimer, come descritto nell'Allen Human Brain Atlas, una mappa dettagliata dell'espressione genica nel cervello umano compilata dall'Allen Human Brain Atlas. Istituto Allen per le scienze del cervello.
«C'era una stretta corrispondenza tra dove si vede un'elevata espressione di APOE e dove si vedono grovigli di tau e danni ai tessuti», ha detto il dottor Gordon, che è anche assistente professore di scienze psicologiche e cerebrali. «E non solo APOE. Se guardate, per esempio, i primi 20 geni associati all'Alzheimer, sono tutti espressi nei lobi temporali in schemi simili. C'è qualcosa di fondamentalmente diverso in queste regioni che le rende vulnerabili al danno cerebrale dell'Alzheimer, e questa differenza è probabilmente insita dalla nascita e influenzata dalla genetica di una persona».
Tutti sono portatori di una versione del gene APOE, ma le persone che portano la variante APOE4 hanno una probabilità fino a 12 volte maggiore di sviluppare il morbo di Alzheimer rispetto alla popolazione generale e in giovane età. I ricercatori dell'Alzheimer sanno da tempo che l'APOE4 aumenta l'accumulo di amiloide-beta nel cervello delle persone. Studiando i topi che sviluppano grovigli di tau ma non placche amiloidi, il dottor David Holtzman, MD (4), la dottoressa Barbara K Burton (5), il professore emerito di neurologia Reuben M. Morriss III e i colleghi hanno dimostrato che l'APOE4 aumenta anche il danno dovuto alla tau, anche senza la presenza di amiloide.
Per valutare l'effetto della variante ad alto rischio di APOE sul danno cerebrale correlato alla tau nelle persone, i ricercatori hanno classificato ogni partecipante come portatore o meno della variante ad alto rischio e hanno analizzato i cluster proteici e l'atrofia nel loro cervello.
«I portatori di APOE4 hanno maggiori probabilità di iniziare ad accumulare amiloide, il che li mette sulla strada dell'Alzheimer», ha detto Gordon. «Quindi, per la stessa quantità di amiloide ottengono più grovigli di tau, il che porta a una maggiore atrofia. È un doppio colpo al cervello».
Nel lavoro futuro, Gordon e colleghi hanno in programma di esplorare in che modo i modelli di espressione genica si relazionano ai modelli di danno tau nelle persone con MA atipico.
«Quando vediamo qualcuno che presenta problemi di vista, c'è una specifica firma genetica che corrisponde alle aree che sono danneggiate nel cervello?» chiese Gordon. «Vogliamo sapere perché alcune persone hanno questi schemi alterati e cosa significa su come si sviluppa l'Alzheimer e come può essere curata».
Dichiarazione COII seguenti autori non hanno interessi in competizione riguardo a questo studio: AD, CDC, NSM, AM, LNK, SF, SJK, RLF, RCH, AMF, JCM e SESSAS ricevono supporto per la ricerca dalla National Science Foundation. BAG riceve supporto per la ricerca dal NIH e dall'Alzheimer's Association NJ-M. è sostenuto in parte dal programma di ricerca internazionale dell'Associazione Alzheimer. CC ha ricevuto sovvenzioni dal NIH e riporta compensi da GSK e Takeda. DMH è cofondatore di C2N Diagnostics LLC e fa parte dei comitati consultivi scientifici o consulta per Genentech, Denali, C2N Diagnostics, Cajal Neurosciences, Takeda, Casma ed Eli Lilly. DMH è un inventore di (i) un brevetto intitolato “Antibodies to tau”, brevetto USA numero 9.834.596, concesso in licenza dalla Washington University a C2N Diagnostics sull'uso terapeutico degli anticorpi anti-tau; e (ii) un brevetto concesso in licenza dalla Washington University a Eli Lilly intitolato “Anticorpo umanizzato che sequestra il peptide beta amiloide”, brevetto statunitense numero 7,892,545, su un anticorpo anti-Aß umanizzato. Il laboratorio di DMH riceve borse di ricerca da NIH, Cure Alzheimer's Fund, Tau Consortium, JPB Foundation, Good Ventures, C2N Diagnostics, NextCure e Denali. TLSB ha finanziamenti per la ricerca avviati dai ricercatori dal NIH, dall'Alzheimer's Association, dalla Barnes-Jewish Hospital Foundation e da Avid Radiopharmaceuticals (una consociata interamente controllata di Eli Lilly). TLSB partecipa come ricercatore in loco a studi clinici sponsorizzati da Avid Radiopharmaceuticals, Eli Lilly, Biogen, Eisai, Jaansen e Roche; è consulente non retribuito di Eisai e Siemens; e fa parte dello Speaker's Bureau for Biogen.
Riferimenti:
(1) APOE e4 genotype, amyloid-ß, and sex interact to predict tau in regions of high APOE mRNA expression
(2) Brian A. Gordon
(3) Institute of Radiology della School of Medicine
(4) David Holtzman
(5) Barbara K Burton
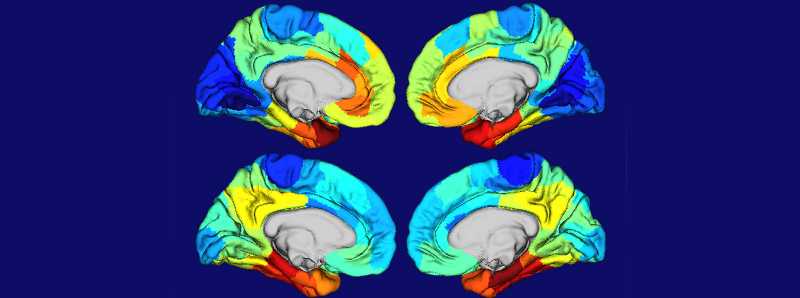
Descrizione foto: Le aree rosse e arancioni su queste mappe di calore del cervello umano mostrano dove il gene APOE è più attivo (le due immagini cerebrali in alto) e dove i grovigli della proteina tau sono più concentrati (le due immagini cerebrali in basso). L'APOE è il più grande fattore di rischio genetico per l'Alzheimer e i grovigli di tau provocano danni cerebrali nella malattia. Le somiglianze nelle due serie di mappe hanno suggerito ai ricercatori della Washington University School of Medicine di St. Louis che l'APOE svolge un ruolo nel rendere alcune aree del cervello particolarmente vulnerabili ai danni dell'Alzheimer. - Credit: Diana Hobbs/Università di Washington.
Autore traduzione riassuntiva e adattamento linguistico: Edoardo Capuano / Articolo originale: Study yields clues to why Alzheimer’s disease damages certain parts of the brain
